آیا متخصصان ژنتیک باید نوزادان بهتری طراحی کنند؟

طی ۹ سال پر از سختی، لسلی و جان براون برای بچهدار شدن تلاش کردند؛ ولی به علت چسبندگی لولههای رحمی، بچهدار نمیشدند. در اواخر ۱۹۷۷ این زوج انگلیسی برای حل این مشکل چشم امیدشان را به دو دانشمند دوختند و بدین طریق حرکتی به سمت مسیری ناشناخته و تاریخی را آغاز کردند. در تاریخ ۲۵ ژولای سال ۱۹۷۸، این زوج به چیزی که مدتها بود آرزو داشتند، دست یافتند؛ لوئیس، نوزاد دختری که تا آن موقع جهان شبیه او را ندیده بود. او از طریق فرایند لقاح آزمایشگاهی یا لقاح مصنوعی (IVF)، روشی که توسط رابرت ادواردز و پاتریک استپتو توسعه یافته بود، پای به این دنیا گذاشت. اسپرم پدر در ظرف آزمایشگاهی با تخمک مادر ترکیب شد و جنین حاصل برای رشد طبیعی در رحم قرار گرفت.

لوئیس براون، نخستین کودک متولدشده با استفاده از تکنیک لقاح مصنوعی به همراه والدینش
لقب کودک آزمایشی بهطور وسیع و البته نادرست در مورد لوئیس به کار گرفته شد. همین برچسب کافی بود تا ذهن میلیونها فرد به سمتی برود که تصور کنند دکتر فرانکنشتاین دارد نقش خدا را بازی میکند و نظم طبیعت را به هم میزند. پس از آن، یک زن اسکاتلندی به نام گریس مکدونالد، در ژانویه ۱۹۷۹ دومین نوزاد آزمایشگاهی را به دنیا آورد؛ نوزادی که نامش را آلیستر گذاشتند. او در مصاحبهای با شبکهی بیبیسی در سال ۲۰۰۳، اعلام کرد که هیچ چیز غیر اخلاقی در این کار وجود نداشت؛ این فقط شبیه گرفتن دستان یک یاریگر بود.
پیشرفتهای مدرنتر در ژنتیک موجب بالا گرفتن مباحث مربوط به مسائل اخلاقی، روحی و سیاسی میشود. اما ببینیم این سوالها در دههی ۱۹۷۰، هنگامی که تکنولوژی لقاح مصنوعی برای نخستین بار معرفی شد، چه بودند: آیا این پیشرفت برای انسانیت سودمند است؟ یا اینها کارهای کفرآمیزی هستند و عواقب ناگواری خواهند داشت؟
لقاح مصنوعی در حال حاضر بهطور عمومی پذیرفته شده است؛ هرچند هنوز هم مخالفانی همچون کلیسای کاتولیک روم وجود دارند. در کل جهان، چیزی حدود ۶ میلیون کودک از این طریق به دنیا آمدهاند و ۳ درصد کل نوزادان در برخی از کشورهای توسعهیافته، حاصل این فرآیند هستند. دکتر پائولو اماتو، استاد مامایی و جراحی در دانشگاه پرتلند، میگوید:
ترس از موضوع کودک طراحیشده با IVF و PGD، در واقع موضوعی افراطی است.
سه درصد کل نوزادان تولدیافته در برخی از کشورهای توسعهیافته، حاصل مصنوعی هستند
PGD، علامت اختصاری برای عبارت «تشخیص ژنتیکی پیش از لانهگزینی جنین در رحم» است که بیش از دو دههی قبل توسعه پیدا کرد و بخشی از لقاح آزمایشگاهی بود. زوجهایی که دارای سوابق خانوادگی بیماریهای جدی مانند فیبروز کیستیک، تیساکس و سندرم داون هستند، میتوانند جنین تولیدشده در آزمایشگاه را از لحاظ احتمالِ به همراه داشتن این اختلالات آزمایش کنند. در واقع تکنولوژی به آنها توانایی کنترل نقص ژنتیکی را میدهد. جنینی که زیر میکروسکوپ «OK» به نظر برسد، میتواند برای رشد طبیعی در رحم مادر کاشته شود (معمولا بقیهی جنینها دور ریخته میشوند و همین از نظر برخی افراد غیر اخلاقی است).
اما اگر موضوع، ممانعت از بیماری کشنده نباشد، چه؟ اگر والدین بخواهند بهجای اینکه مثل گذشته اجازه بدهند جنسیت فرزند شانسی باشد، خودشان بخواهند جنسیت را تعیین کنند؟ دکتر جفری استینبرگ مدیر مؤسسهی باروری در نیویورک میگوید این موضوع اگر برای والدین اهمیت داشته باشد، میتواند همراه با تشخیصهای قبل از لانهگزینی انجام شود. دکتر استینبرگ میگوید:
در مرحله اول این تشخیص صرفا در مورد بیماریهای ژنتیکی بود؛ اما من تصمیم گرفتم آن را گسترش بدهم و این چیزی است که مردم دوست دارند و موجب ضرری نمیشود و موجب خوشحالی مردم هم میشود.
بسیاری از پزشکان از این رویه شاکی هستند؛ ولی استینبرگ حتی برای افزایش احتمال اینکه فرزند دارای رنگ چشم دلخواه باشد، این تشخیص را پیشنهاد میدهد. البته بهجز اینها، تکنیکهای تغییر ژنتیکی دیگری نیز در حال ایفای نقش هستند. انتقال میتوکندریایی برای زنانی است که پبشینهی ژنتیکی آنها موجب میشود فرزندی با نقص ژنتیکی شدیدی به دنیا بیاید (یعنی ژنهای مربوط به ژنوم میتوکندری آنها حامل اطلاعات بیماری هستند).
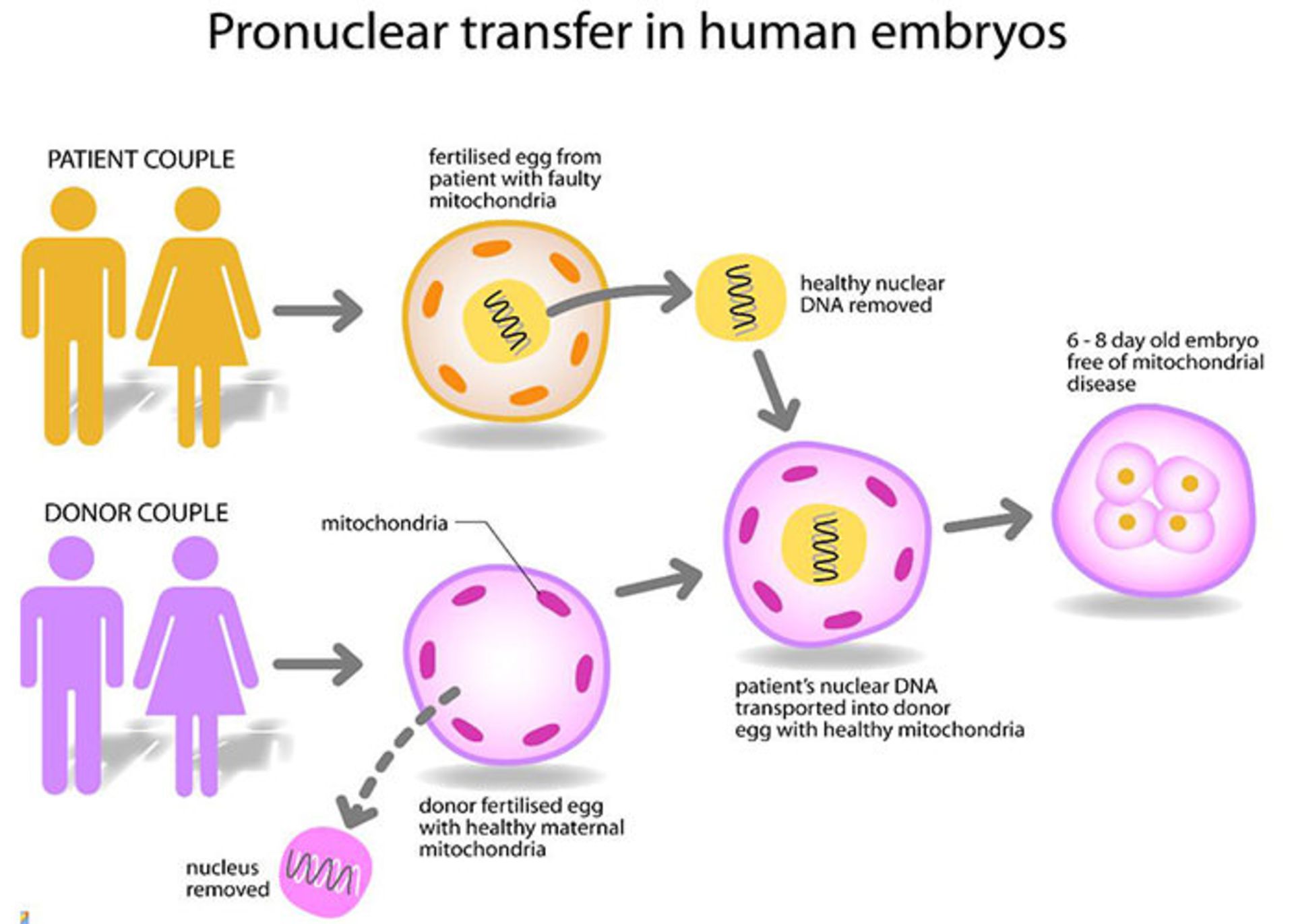
DNA از تخمکِ زنی که دارای مشکلات ژنوم میتوکندری است، خارج میشود و به تخمک زن دیگری که دارای اجزای تولیدکننده انرژی سالم در میتوکندری است، منتقل میشود (میتوکندیها که در سیتوپلاسم سلول قرار دارند تنها از طریق مادر به فرزند منتقل میشوند)؛ اصطلاح «کودک دارای سه والد» از اینجا مطرح شده است. مراحل انتقال میتوکندری در شکل زیر نشان داده میشود؛ محتویات ژنتیکی هسته تخمک مادری که ژنوم میتوکندری او حامل بیماری است، از سیتوپلاسم جدا و وارد یک سیتوپلاسم بدون هسته زن دیگری میشود که دارای مشکلی در ژنوم میتوکندری نیست.
روش دیگر، روش ویرایش ژنی با نام کریسپر است. گروهی از پژوهشگران تحت هدایت علمی میدالی پو، متخصص زیستشناسی باروری، سال پیش اعلام کردند که از این تکنیک برای تغییر ژنوم یک انسان استفاده کردهاند.آنها با استفاده از آنزیمی به نام Cas9 که بهعنوان یک بُرنده (قیچی ژن) عمل میکند، یک ژن جهشیافته را که موجب ضخیم شدن ماهیچههای قلبی و مرگ ناگهانی ورزشکاران میشود از ژنوم یک انسان جدا کردند.
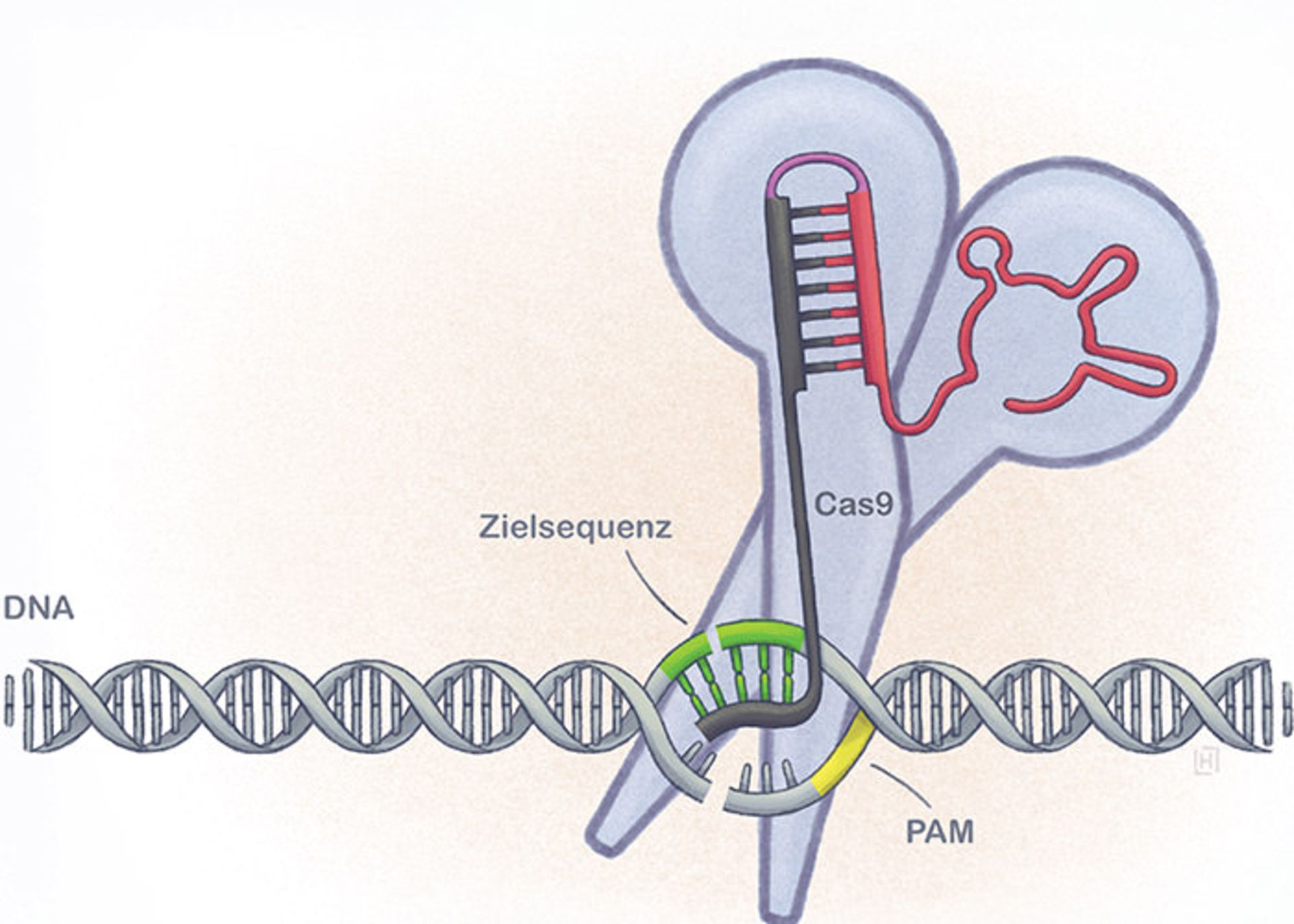
دانشمندان با روش کریسپر یک ژن جهشیافته را که موجب ضخیم شدن ماهیچههای قلبی و مرگ ناگهانی ورزشکاران میشود، از ژنوم یک انسان جدا کردند
از نظر تئوری اگر جنینی با چنین ژن تغییریافتهای در رحم کاشته شود (چون این قسمت کار در پروژهی کریسپر مذکور نبود)، نوزاد متولدشده آن جهش را با خودش نخواهد داشت و در ادامه نسل، این ژن معیوب منتقل نمیشود. بهطور خلاصه میتوان گفت با این کار، مادهی ژنتیکی این خانواده که از نسلی به نسل دیگر منتقل میشود، بهطور دائمی تغییر مییابد.
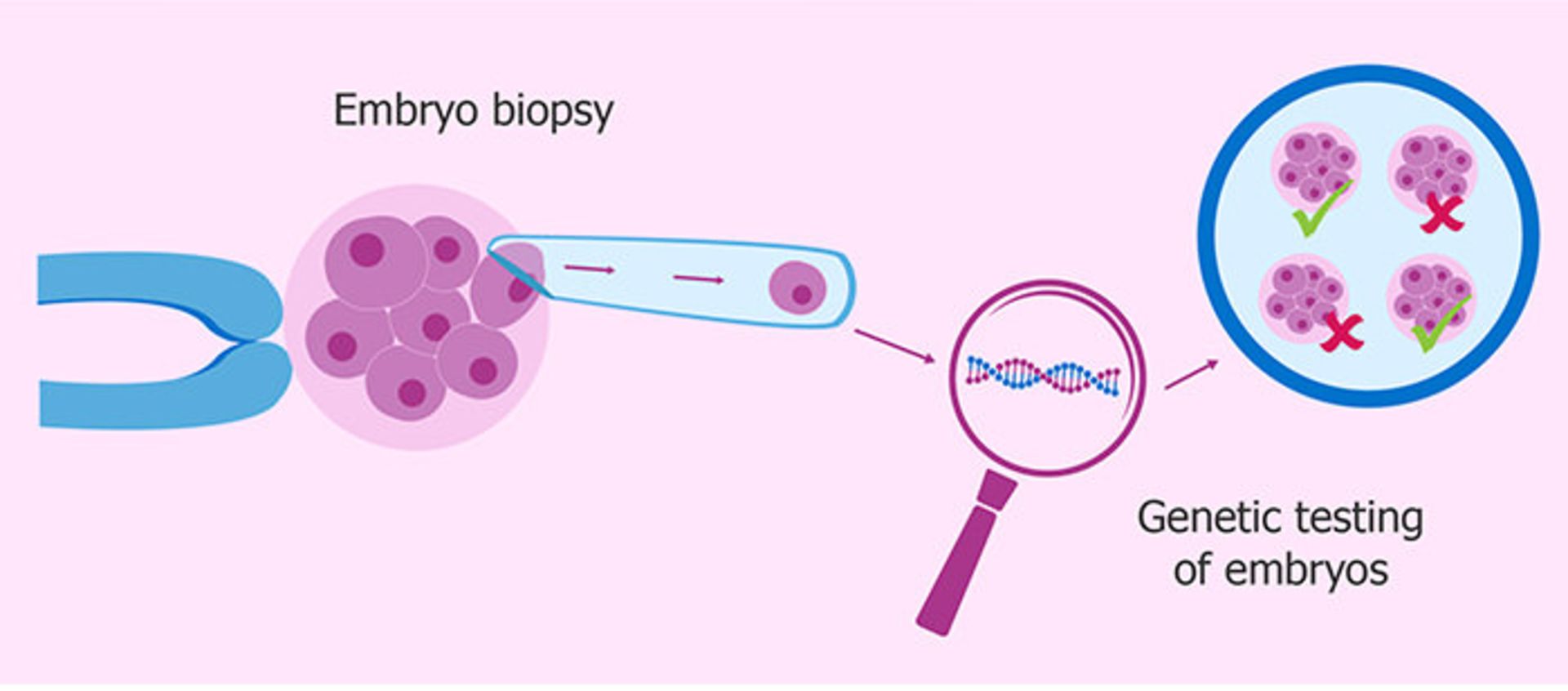
طی تشخیصهای ژنتیکی پیش از لانهگزینی، جنینی که زیر میکروسکوپ «OK» به نظر برسد، برای رشد طبیعی در رحم مادر کاشته شود و بقیه دور ریخته میشوند
برخی اخلاقگرایان تنها جنبهی خوب حذف بیماریهایی که موجب بدبختی خانوادهها میشود، میبینند؛ مگر در واکسیناسیون هم از تکنولوژی برای همین هدف استفاده نمیشود؟ افرادی معدودی تزریق واکسن علیه سرخک یا فلج اطفال را چیزی میدانند که در حال بر هم زدن نظم دنیا است. نگاه برخی افراد به این قضیه متفاوت است؛ آنها به دنبال این هستند که استفاده از روش ویرایش ژن برای اهداف دیگری بهغیر از مبارزه با بیماریها استفاده نشود؛ مثلا برای طراحی انسانهایی که قویتر و یا باهوشتر از بقیه باشند و نیز افرادی که میخواهند فرزندی به دنیا بیاورند که برای داشتن هوش بالا برنامهریزی ژنتیکی شده باشد. از سوی دیگر هزینههای گزاف این فرآیندها ممکن است موجب افزایش فاصله بین ثروتمندان و دیگران شود. البته انتخاب ژنها برای اینکه مثلا یک بازیکن بسکتبال به وجود آید، آسان نیست؛ قد انسان بهتنهایی تحت تأثیر دهها هزار واریانت ژنتیکی است.
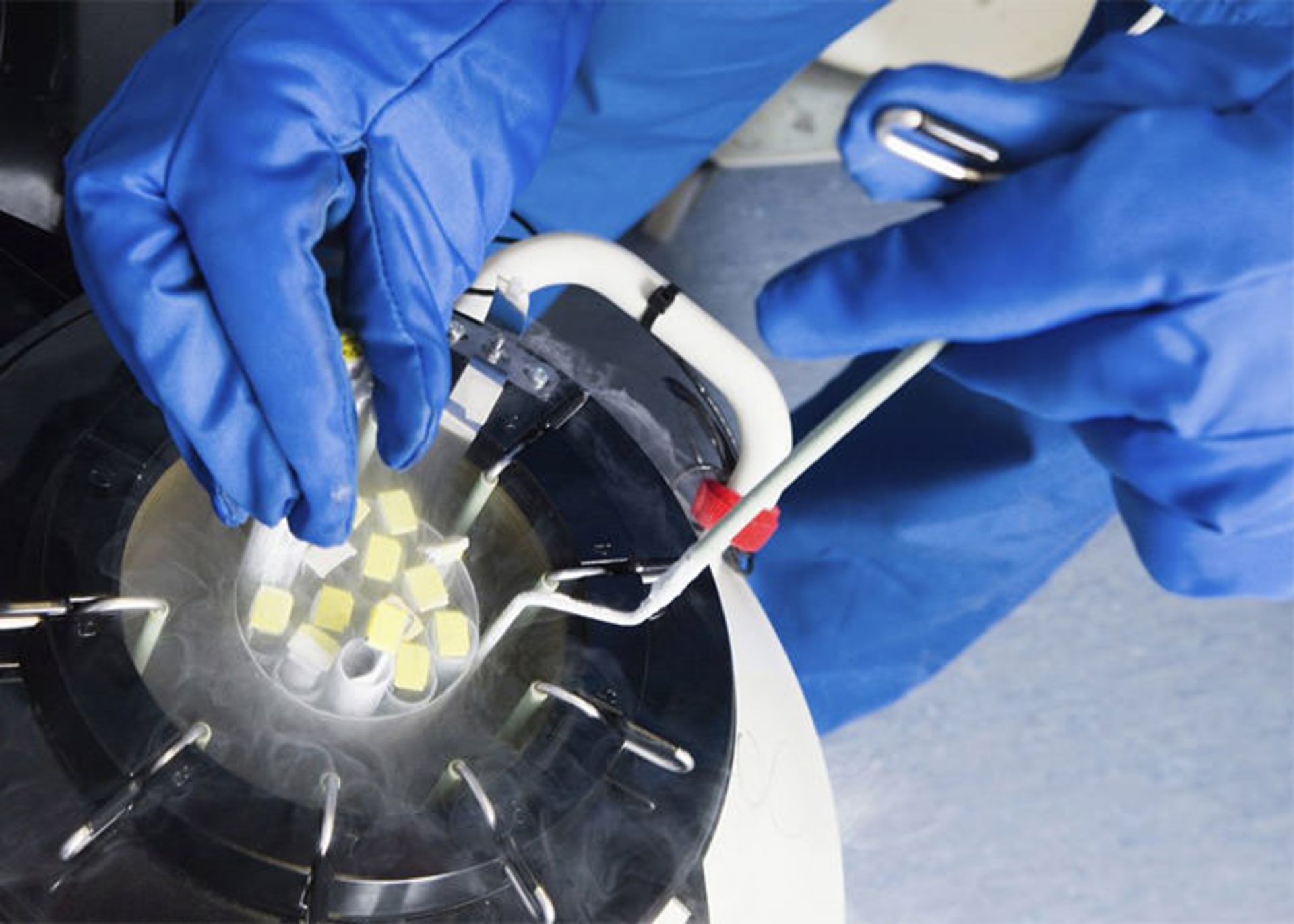
گروهی از دانشمندان تأیید کردند که از مهندسی تخمک، اسپرم و جنین تنها با هدف پیشگیری از تولد نوزادانی با ژنهای مسبب بیماریهای جدی و معلولیت استفاده کنند
در سال ۲۰۱۷، گروهی از آکادمی ملی علوم و آکادمی ملی پزشکی توافقنامهای در مورد اصول ویرایش ژنی امضا کردند؛ با این شرط که فقط در مقابله با بیماریهای جدی و معلولیت هنگامی که چارهی دیگری موجود نیست، استفاده شود. برخی دانشمندان هم میگویند عاقلانه نیست که به خاطر ترس از ناشناختهها فلج شویم. اما مارسی دارنوسکی مدیر اجرایی مرکز ژنتیک و جامعه تردید بیشتری دارد. او میگوید:
ما باید بپرسیم نقطه توقف کجا است. علاوه بر دانشمندان، لازم است پلیس نیز در این زمینه حرفهایی بزند.





