چگونه چاقی و مقاومت به انسولین موجب اختلال در عملکرد شناختی مغز میشوند
پژوهشگران میدانند که فعال شدن مزمن گیرندههای Adora2a موجود روی سلولهای اندوتلیال پوشانندهی سد خونی-مغزی، به مولکولهای زیادی اجازهی ورود به مغز را میدهند و روی عملکرد نورونها تاثیر میگذارند. بهتازگی دانشمندان کالج پزشکی جورجیا نشان دادهاند که با مهار Adora2a در یک مدل چاقی ناشی از رژیم غذایی، عملکرد این سد مهم حفظ میشود. دکتر الکسیس استرانهان، دانشمند علوم اعصاب دانشگاه آگوستا میگوید:
ما میدانیم که چاقی و مقاومت به انسولین در انسانها و مدلهای حیوانی موجب اختلال در سد خونیمغزی میشود اما چگونگی این فرایند هنوز درک نشده است.مقالههای مرتبط:دیابت یا بیماری قند: از علائم بیماری تا درمان آنبدن ما در آینده میتواند دیابت را درمان کندکاهش خطر ابتلا به دیابت نوع ۲ با مصرف ویتامین D
آدنوزین یکی از ناقلهای عصبی موجود در مغز است که به ما کمک میکند بخوابیم و نیز به تنظیم فشار خون کمک میکند. آدنوزین همچنین یکی از اجزای تشکیلدهندهی سوخت سلول یا آدنوزین تریفسفات (ATP) است. آدنوزین همچنین موجب فعالشدن گیرندههای Adora1a و Adora2a موجود روی سلولهای اندوتلیالی میشود که بهطور طبیعی از روابط سالم بین فعالیت مغز و جریان خون حمایت میکنند. استرانهان میگوید:
مشکلاتی که با فعال شدن مزمن این گیرندهها در مغز اتفاق میافتد، همان چیزی است که در چاقی رخ میدهد.
افرادی که دچاری چاقی و دیابت هستند، با افزایش سن، بیشتر درگیر مشکلات شناختی میشوند و تغییرات ساختاری در هیپوکامپ مغز آنها که مرکز یادگیری و حافظه است، رخ میدهد.
چربی یکی از منابع التهاب است و شواهدی وجود دارد که نشان میدهد کاهش التهاب مزمن در مغز به پیشگیری از ضعف حافظهی ناشی از چاقی کمک میکند. در مدلی که تقلیدی از همان چیزی است که برای برخی از انسانها اتفاق میافتد، موشهای جوان با رژیمهای غذایی سرشار از چربی تغذیه و طی مدت ۲ هفته چاق شدند و در هفتهی ۱۶ سطح گلوکز ناشتا و غلظت انسولین آنها بهعنوان مقدمهای از دیابت افزایش یافت.
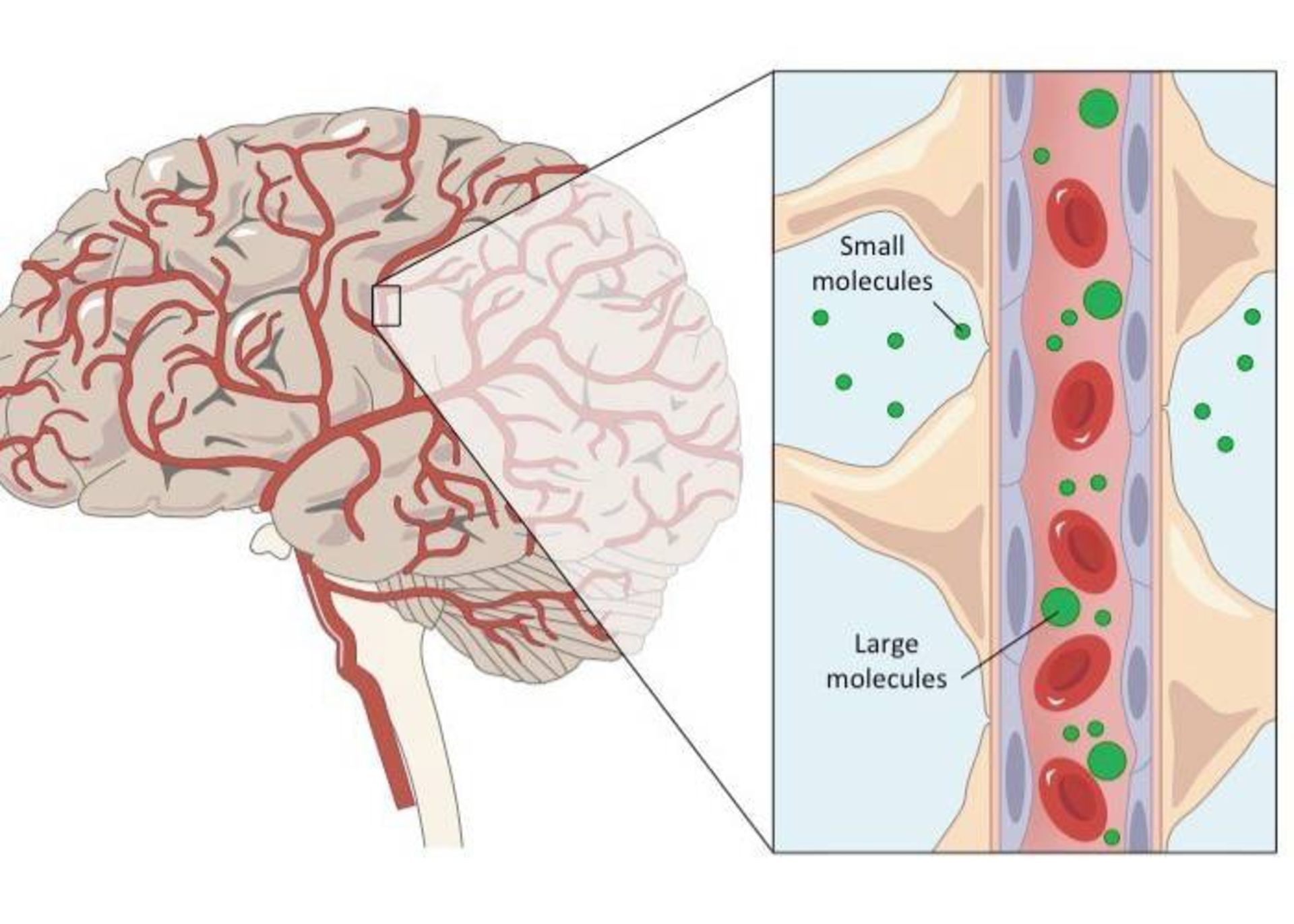
چیزی که پژوهشگران مشاهده کردند این بود که در سطح عروق خونی ریز موجود در هیپوکامپ، چاقی نخست میزان نفوذپذیری سد خونیمغزی را دربرابر مولکولهای کوچکی نظیر NaFl افزایش داد. مقاومت نسبتبه انسولین ناشی از رژیم غذایی موجب افزایش این نفوذپذیری شد و در ادامه مولکول بزرگتری نظیر آبی اوانز نیز که دارای گرایش بالایی به آلبومین (فراوانترین پروتئین موجود در خون) است، نیز توانست از سد خونیمغزی عبور کند. هنگامی که پژوهشگران با استفاده از میکروسکوپ الکترونی سد خونیمغزی را مورد بررسی قرار دادند، منظرهی متفاوتی دیدند: دیابت موجب شل شدن اتصالات محکم بین سلولهای اندوتلیال و حفرههای حقیقی بین این سلولها شده بود.
علاوهبر این سلولهای ماهیچهای که پریسیت نامیده میشوند و لایهی خارجی عروق خونی مغز را میپوشانند و موجب استحکام آنها شده و به جریان خون کمک میکنند، استحکام خود را از دست داده بودند. در این وضعیت حالت ارتجاعی عروق خونی از بین رفته و عملکرد آنها دچار مشکل شده بود. همچنین نشانههایی از التهاب نیز دیده میشد.
دانشمندان از این موضوع آگاهی دارند که میزان بیان Adora2a در سلولهای ماهیچهای پریسیت نسبتبه سلولهای اندوتلیال بیشتر است. رژیم غذایی حاوی چربی بالا همچنین موجب تورم برجستگیهای موجود روی آستروسیتها میشود. این برجستگیها که پاهای انتهایی نامیده میشوند نیز بخشی از سد خونیمغزی هستند. آستروسیتها گروهی از سلولهای موجود در مغز هستند که بهطور طبیعی نورونها را پرورش میدهد اما وضعیت پاتولوژیکی چاقی موجب تغییر در شکل و نقش حمایتی آنها میشود.
در هفتهی ۱۲ و در پاسخ به نقص در جریان خون و اکسیژنرسانی به هیپوکامپ، در این منطقه از مغز آنژیوژنز (رگزایی) دیده میشد و عروق خونی نیز ملتهب شده بودند. با استفاده از دارویی که بهطور موقت موجب مهار Adora2a میشد، مشکلات مرتبط با نفوذپذیری سد خونیمغزی نیز از بین رفت. اینکه آیا این روش میتواند در انسانها و طی بلندمدت بهعنوان راهی برای ممانعت از زوال شناختی در افراد چاق مورد استفاده قرار گیرد، چیزی است که بهعقیدهی استرانهان باید مورد بررسی بیشتر قرار گیرد.
پژوهشگران در ادامهی مطالعهی خود موشهایی تولید کردند که میتوانستند در آنها بهطور انتخابی گیرندههای Adora2a را غیرفعال کنند. آنها این گیرندهها را در این موشهای ترانسژنیک در هفته ۱۲و ۱۶ یعنی زمانیکه موشها باید دچار نقص شناختی و ضعف سد خونیمغزی میشدند، غیرفعال کردند. با انجام این کار، این موشها دارای عملکرد شناختی طبیعی بودند و علاوهبر اینکه اثری از التهاب دیده نمیشد، سد خونیمغزی آنها نیز ضعیف نشد.
پژوهشگران با مقایسهی موشهای ترانسژنیکی که تحت رژیمهای غذایی پرچربی و کمچربی قرار گرفته بودند، دریافتند که افزایش نفوذپذیری عروق خونی مغز، آغازگر چرخهی التهاب و تضعیف عملکرد شناختی است. استرانهان میگوید:
«در حالیکه بهراحتی نمیتوان این نتایج را به انسانها تعمیم داد، ولی این واقعیت که این نوع پژوهش در ابتدا با کار روی انسان آغاز شده، احتمالا به این مفهوم است که جلوگیری از ایجاد مقاومت به انسولین میتواند مانع از افزایش نفوذپذیری سد خونی-مغزی و کاهش زوال عملکرد شناختی در انسان شود. اگر هم فردی نسبتبه انسولین مقاومت حاصل کرده است، این نتایج بر اهمیت کنترل سطوح قند خون و جلوگیری از رسیدن به مرحلهی کمبود انسولین (دیابت) که موجب تضعیف بیشتر سد خونیمغزی میشود، تاکید میکند.»
بهعقیدهی پژوهشگران، دسترسی نسبی به عروق خونی مغز ممکن است آنها را مسیر مناسبی برای ممانعت از رسیدن اثرات چاقی به مغز تبدیل کند. این وضعیت همچنین به این واقعیت اشاره میکند که داروهایی که به افراد چاق داده میشود، ممکن است روی مغز آنها تاثیر بیشتری داشته باشد و این موردی است که بیمار و پزشک باید مد نظر قرار دهند. استرانهان به این نکته نیز اشاره میکند که برای داروهایی که قرار است روی مغز تاثیر بگذارند، مانند داروهای آلزایمر، این وضعیت میتواند چیز خوبی باشد ولی باید مورد بررسی بیشتر قرار گیرد. او میگوید:
از طرف دیگر برخی از داروهای تجویزی معمول نظیر پردنیزون، بهخوبی میتوانند از این سد عبور کنند و ممکن است حتی برای مغز بد باشند.
هدف بعدی این پژوهشگران این است که بدانند سیگنالهایی که بهطور مزمن موجب فعال شدن گیرندههای Adora2 موجود در چربی موشها میشوند، از کجا میآیند. استرانهان حدس میزند که این فرایند با وارد شدن تنش به سلولهای اندوتلیال آغاز میشود. درنتیجهی این امر، میزان متابولیسم آنها افرایش مییابد. افزایش متابولیسم بهمعنای مصرف مقدار بیشتری از ATP است و این بهنوبهی خود موجب فعال شدن گیرندههای Adora2a و به حرکت درآمدن چرخهی معیوبی میشود که درنهایت بار خود را بر سد خونیمغزی تحمیل میکند.
این ایده که چاقی میتواند روی سد خونیمغزی تاثیر بگذارد، چندین سال پیش و از زمان کار روی انسانها آغاز شد، وقتی پژوهشگران سوئدی متوجه شدند سطوح آنتیبادی ایمونوگلوبولین G در مایع مغزینخاعی افراد چاق بیشتر است درحالیکه چنین حالتی باید در جریان خون آنها وجود داشت و نه مایع مغزینخاعی. استرانهان میگوید این یافتهی مهمی بود که نشان میداد چاقی و دیابت میتوانند موجب شوند موادی که نباید وارد مغز شوند، راه خود را به مغز پیدا کنند. مطالعات حیوانی نیز این موضوع را تأیید کردهاند ولی باز باید گفت مطالعات کمی در مورد علت آن انجام شده است.
عروق خونی از بدن میآیند و وقتی به مغز میرسند، بسیار کوچک و ضعیف میشوند. درحالیکه عروق خونی که مناطقی نظیر بازوها و قلب ما را تغذیه میکنند، باید بسیار متخلل باشند که بتوانند مقدار زیادی گلوکز، اکسیژن و سلولهای ایمنی و دیگر مواد مورد نیاز بدن را به این بخشها برسانند، بافت عروق خونی مغز باید بسیار محدودتر باشد تا اجازهی ورود هر نوع مادهای را به مغز ندهد.
استرانهان این مانع را بهصورت یک سد پویا توصیف میکند که براساس عملکرد مغز اجازه ورود به برخی از مولکلولها را میدهد. چیزی که در مغز و در خون اتفاق میافتد، میتواند روی نحوهی عمل این سد تاثیر بگذارد. او خاطر نشان میکند که مغز یک مصرفکنندهی بزرگ است و ۸۰-۷۰ درصد از اکسیژن و گلوکز ما را مصرف میکند ولی در عین حال حساستر و شکنندهتر از بافتهای دیگر بدن است و حتی دربرابر سلولهای ایمنی بدن نیز حساس است.
آزمایشهای شناختی که در این مطالعه روی موشها انجام شد، شامل شناخت اشیاء و حرکت در یک مارپیچ آبی بود. دانشمندان به دیگر عملکردهای طبیعی مانند عملکردهای حرکتی ساده نیز توجه کردند تا ببینند که آیا تاثیرات دیگری نیز دیده میشود یا نه ولی حداقل در این مرحله از زمان آنها تغییر دیگری مشاهده نکردند.