استفاده از کریسپر برای از بین بردن مخازن پنهان ویروس ایدز در بدن
پژوهشگران دانشگاه کالیفرنیا آغازگرهای سلولی را درون سلولهای ایمنی پیدا کردهاند که میتوانند جهت کشتن مخازن خفتهی HIV-1 در افراد مبتلا به عفونت این ویروس تحت کنترل درآیند. این یافتهها پیشرفتی در درک مکانیسمهای سلولی کنترلکنندهی تکثیر HIV درون بدن است و میتواند منجر به توسعهی اهداف دارویی و درمانهایی شود که مخازن HIV درون بدن را نابود کنند. نتایج این پژوهش در مجلهی mBio منتشر شده است.
براساس گزارشهای سال ۲۰۱۸، ویروس نقص ایمنی انسانی نوع یک (HIV-1) هر ساله ۱/۷ میلیون فرد جدید را آلوده میکند و در حال حاضر حدود ۳۸ میلیون نفر در سرتاسر جهان با این عفونت زندگی میکنند. ریشهکن کردن مخازن پایدار HIV-1 در بدن مانع اصلی بر سر راه دستیابی به درمانی برای این بیماری است. طارق رانا، نویسندهی مقاله میگوید:
سه دهه است که پژوهشگران حوزهی HIV بهدنبال دستیابی به چنین کلیدی (برای ازبینبردن ویروسهای پنهان) بودهاند. هیجانانگیزترین بخش این کشف، تا قبل از این، هرگز دیده نشده بود. ما با تغییر ژنتیکی قطعهی بلندی از RNA غیرکدکننده، از بازگشت HIV به سلولهای T و میکروگلیاها پس از قطع درمان ضدرتروویروسی پیشگیری کردیم. این امر نشان میدهد که ما یک هدف درمانی بالقوه برای ریشهکن کردن HIV و ایدز پیدا کردهایم.
نمایشی از ویروس HIV
ویروس HIV ازطریق مایعات بدن منتشر شده و با حمله به سیستم ایمنی منجر به نقص ایمنی یا ایدز میشود. داروهای ضدرتروویروسی یا ART بهمنظور پیشگیری از انتشار عفونت و نیز تکثیر HIV درون بدن، بهصورت ترکیبی به بیماران داده میشود. این داروها مانع از تبدیل عفونت به ایدز میشوند. این ویروس در بدن فردی که داروها را دریافت میکند، بهحالت خفته باقی میماند و از بین نمیرود. بهمحض قطع رژیم درمانی، ویروس شروع به تکثیر میکند و بیماری را بازمیگرداند.
بهگفتهی پژوهشگران، یک چالش مهم در مسیر یافتن درمانی برای HIV و ایدز، دشواری شناسایی و ریشهکن کردن مخازن همیشگی پروویروسهای دارای قابلیت تکثیر است. پژوهشگران دریافتند که ماکروفاژها یا سلولهای ایمنی آلوده به HIV حاوی یک قطعهی طولانی RNA غیرکدکننده (lncRNA) هستند که از بیش از ۲۰۰ نوکلئوتید تشکیل شده است. آنها بیش از ۱۱۴۵ نمونه lncRNA را توالییابی کردند. این RNAها از این جهت خاص هستند که مانند دیگر RNAها کدکنندهی پروتئین نیستند و مانند کلیدی برای کنترل ژنهای دیگری که سنتز پروتئینهای خاصی را تنظیم میکنند، عمل میکنند.
پژوهشگران یک lncRNA خاص با نام HEAL را پیدا کردند که در افرادی که دچار عفونت HIV بودند، سطح آن افزایش یافته بود. HEAL تکثیر HIV را در سلولهای ایمنی نظیر ماکروفاژها، سلولهای T و میکروگلیاها تنظیم میکند.
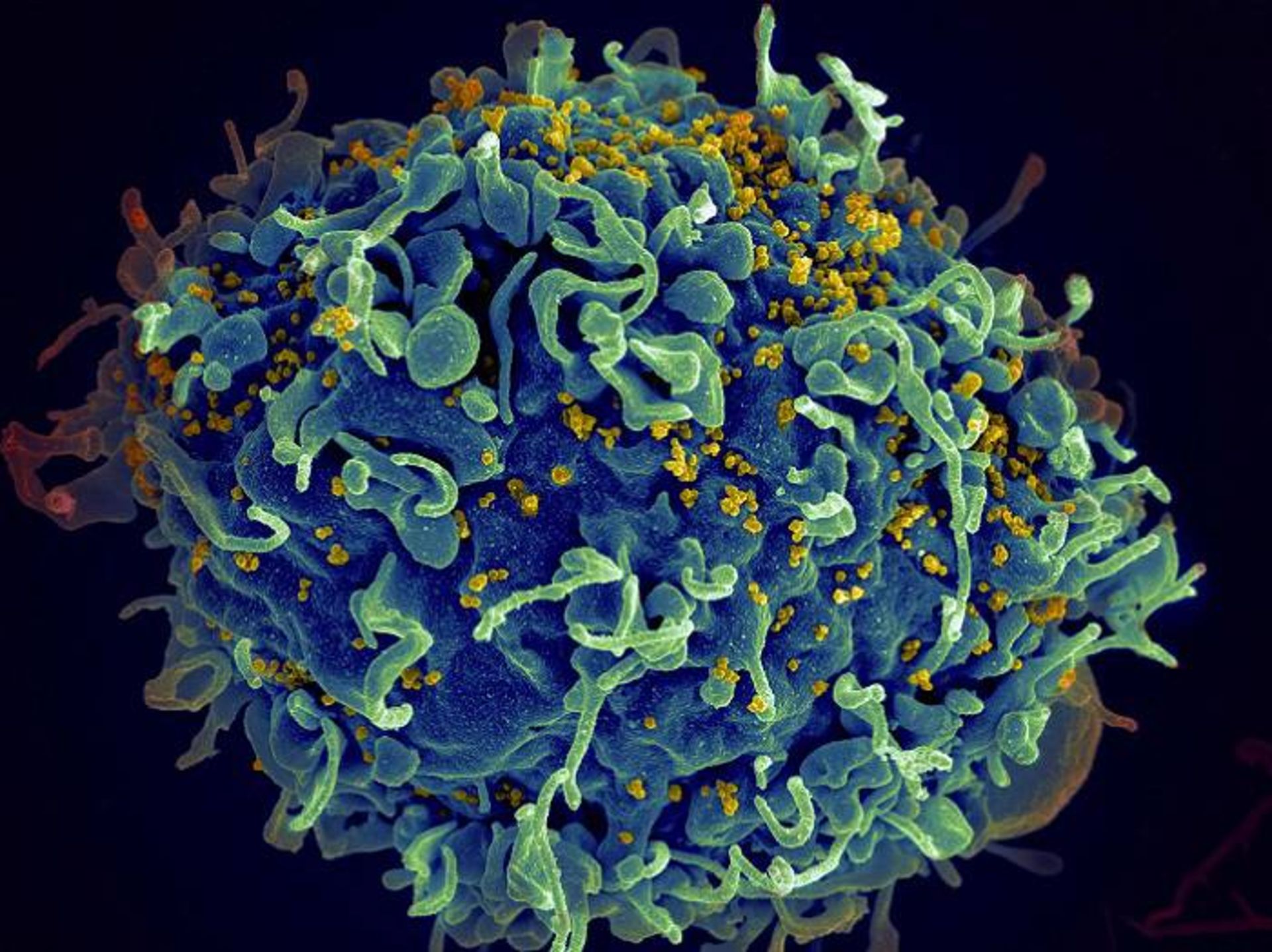
یک سلول انسانی آلوده به ویروس HIV
پژوهشگران توضیح دادند که HEAL با یک پروتئین متصلشونده به RNA که FUS نام دارد، کمپلکسی را تشکیل میدهد. این پروتئین ازطریق دو مکانیسم به تکثیر HIV کمک میکند. مکانیسم اول، پیوند کمپلکس HEAL-FUS به یک پروموتر HIV است که باعث افزایش فعالیت آنزیم هیستون استیل ترانسفراز p300 میشود که فعال شدن تکثیر HIV را بهدنبال دارد. مکانیسم دوم آن است که کمپلکس HEAL-FUS روی منطقهی پروموتر ژن کیناز وابسته به حلقه (CDK2) عمل میکند و موجب افزایش بیان این ژن میشود.
پژوهشگران در مرحلهی بعد، روی خاموشکردن HEAL با استفاده از ابزارهای بیوشیمیایی، سلولی و ژنتیکی کار کردند. آنها از مهار RNA برای خاموشکردن HEAL استفاده کردند و نیز سعی کردند، HEAL را با استفاده از ابزار ویرایش ژن کریسپر و به کمک آنزیم Cas9 ویرایش یا حذف کنند. بهمحض اینکه HEAL از صحنه خارج شد، ویروس HIV حتی پس از توقف مصرف داروهای ضدرتروویروسی قادر به بازگشت نبود. پژوهشگران توضیح دادند:
HEAL یک تقویتکنندهی پردامنه از چندین سویه از HIV-1 است؛ زیرا حذف HEAL موجب ممانعت از تکثیر X4، R5 و ویروس دوگانهی HIV میشد و این تأثیر بازدارندگی با بیان بیش از حد HEAL از بین میرفت.
پژوهشگران قصد دارند آزمایش خود را از سطح ظروف آزمایشگاهی خارج کنند و مطالعات حیوانی انجام دهند. رانا گفت:
نتایج ما نشان میدهد که HEAL نقشی حیاتی در بیماریزایی HIV دارد. برای توضیح مکانیسمی که پس از آلودهشدن یک فرد با HIV منجر به بیان HEAL میشود، نیاز به مطالعات بیشتری است اما از این نتایج میتوان برای ایجاد یک هدف درمانی استفاده کرد.
پژوهشگران در مطالعهی خود چنین نتیجهگیری کردند:
درک ما از عملکردهای lncRNA افزایش یافته است، اما هنوز پتانسیل آنها برای توسعهی استراتژیهای درمانی برای HIV و ایدز ناشناخته مانده است. HEAL برای افزایش به کارگیری کمک فعالکنندهی رونویسی p300 روی پروموتر HIV، با پروتئین متصلشونده به DNA یعنی FUS کمپلکسی را تشکیل میدهد. HEAL میتواند هدف درمانی برای درمان عفونت HIV و ایدز باشد.