موفقیت دانشمندان در بازسازی سلولهای عصب بینایی موش در آزمایشگاه
آسیب دیدن سلولهای عصب کاملا رشدیافته، پیامدهای بازگشتناپذیر و تغییردهندهی زندگی به همراه دارد؛ زیرا وقتی تارهای عصبی بالغ میشوند، توانایی بازسازی پس از آسیب یا بیماری را از دست میدهند. آزمایشهای جدید نشان میدهد که نحوهی فعال شدن بخشی از دستگاه احیاکنندهی سلول عصبی - که پروتئینی است که پروترودین نام دارد - میتواند اعصاب چشم را تحریک کند تا پس از آسیب مجددا رشد کنند.
با پژوهشهای بیشتر، این دستاورد گامی به سوی درمانهای آینده گلوکوم است که گروهی از بیماریهای چشم هستند که با آسیب رساندن به عصب بینایی - که چشم را به مغز متصل میکند - باعث از دست دادن بینایی میشوند. کیت مارتین، چشمپزشک دانشگاه ملبورن استرالیا، میگوید: «قبلا بازسازی عصب بینایی غیر ممکن به نظر میرسید؛ اما پژوهش ما پتانسیل ژندرمانی را برای انجام این کار نشان میدهد.»
البته پیشازاین شاهد تلاشهایی برای بازگرداندن بینایی موشها و برخی نتایج امیدوارکننده بودهایم. در سال ۲۰۱۶، دانشمندان با فعال کردن یک کلید رشد غیرفعال توانستند بخش کمی از سلولهای گانگلیونی شبکیه را در موشهای بالغ دوباره رشد دهند و نشان دادند که سلولهای جدید در پشت چشم بهسمت راست مغز متصل شدهاند. قبل از آن، مطالعهای در سال ۲۰۱۲ تا حدی بینایی ساده موشهای بالغ را پس از بازسازی اعصاب در تمام طول مسیر بینایی بازیابی کرد. جدیدترین پژوهش در این زمینه هنوز در مراحل ابتدایی قرار دارد و روی درک دقیق نحوهی عملکرد پروترودین برای حمایت از رشد سلول تمرکز کرده است. همیشه داشتن چند گزینه خوب است؛ زیرا هیچ تضمینی وجود ندارد که نتایج امیدوارکننده در مطالعات موش به درمانهای مؤثر و بیخطری برای انسان تعبیر شود.
دانشمندان در مطالعهی جدید، سلولهای عصبی چشم را تحریک کردند تا پروترودین بیشتری تولید کنند تا ببینیدو آیا این امر به محافظت از سلولها در برابر آسیب و ترمیم پس از آسیبدیدگی کمک میکند یا نه. پژوهشگران در آغاز در سلولهای عصب بینایی که در ظرفی کشت داده شده بودند، نشان دادند افزایش تولید پروترودین موجب تحریک بازسازی سلولهای عصبی میشود که بهوسیلهی لیزر بریده شدهاند. آکسونهای دوکمانند آنها نسبت به سلولهای تیمارنشده، در فواصل طولانیتر و در زمان کمتری احیا شدند.
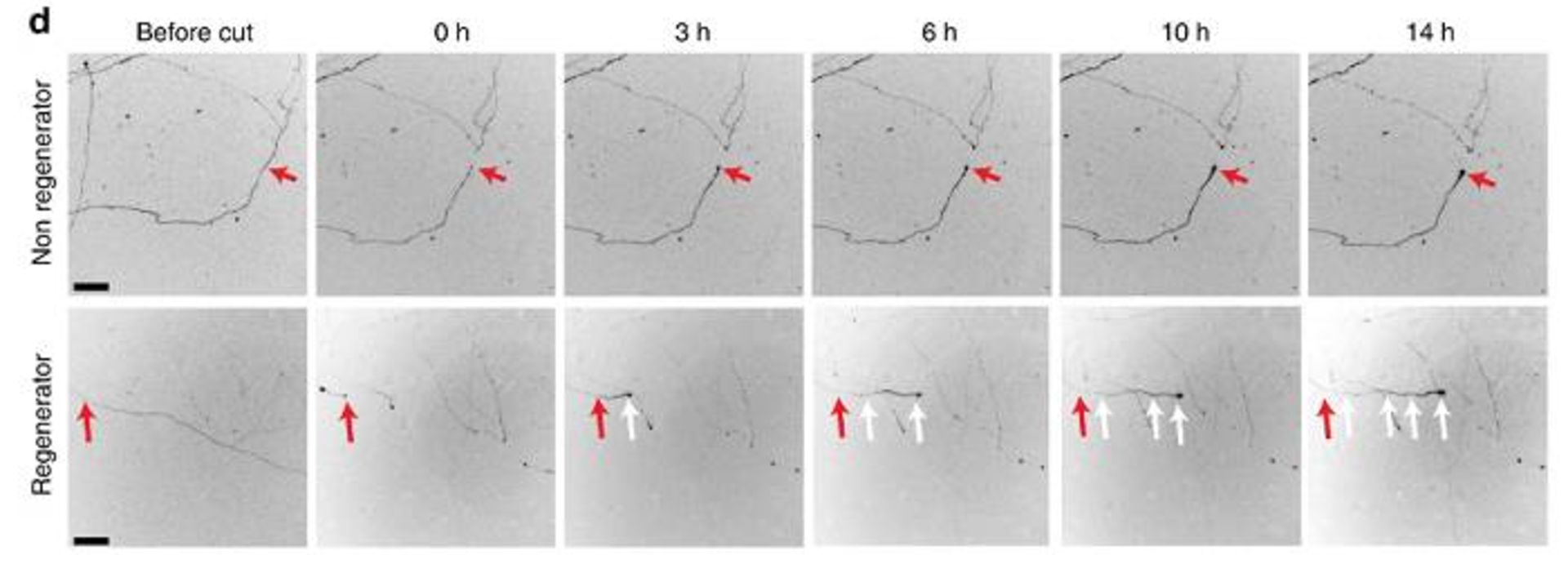
یک آکسون احیاشونده و یک آکسون غیر احیاشونده طی ۱۴ ساعت از آکسوتومی با استفاده از لیزر. پیکانهای قرمز در صفر ساعت پس از جراحت، نقطهی آسیبدیدگی را نشان میدهند و پیکانهای سفید مسیر آکسونهای احیاشونده را دنبال میکنند
سپس موشهای بالغ تحت ژندرمانی قرار گرفتند (تزریق مستقیم به چشم) که دستورالعمل افزایش تولید پروتئین پروترودین را حمل میکرد. پس از گذشت چند هفته، موشهایی که دچار آسیب عصب بینایی شده بودند و تحت ژندرمانی قرار گرفته بودند، نسبت به گروه کنترل سلولهای عصبی بازمانده بیشتری در شبکیهی خود داشتند.
در آخرین آزمایش، دانشمندان برای تأیید اثر محافظتی پروترودین در ممانعت از مرگ سلولهای عصبی، از کل شبکیهی چشم موش استفاده کردند. آنها متوجه شدند تحریک تولید پروترودین تقریبا از نورونها محافظت کرده است و این شبکیهها هچ کاهشی در نورونهای خود نشان ندادند. معمولا حدود نیمی از نورونهای شبکیهای که به این روش برداشته میشود، طی چند روز از بین میروند. وسلینا پترووا، دانشجوی علوم اعصاب دانشگاه کمبریج، میگوید: «استراتژی ما متکی بر استفاده از ژندرمانی برای تحویل پروترودین به چشم است (رویکرد ژندرمانی اکنون مورد استفادهی بالینی قرار دارد). ممکن است درمان ما بهعنوان روشی برای محافظت از نورونهای شبکیه در برابر مرگ و نیز تحریک رشد مجدد آکسونهای آنها توسعه پیدا کند.»
توجه به این مسئله مهم است که هنور با بازیابی بینایی فرد فاصلهی زیادی داریم: بازسازی سلولها در ظرف آزمایشگاهی عالی است؛ اما از این آزمایشها متوجه نمیشویم آیا اگر به موش پروترودین بیشتری بدهیم، بیناییاش بازمیگردد. یکی از مراحل بعدی بررسی این موضوع خواهد بود که آیا پروترودین در سلولهای شبکیه انسانی کشتشده نیز همان اثر محافظتی را دارد. دانشمندان منتشرکنندهی مقاله همچنین قصد دارند ببیند آیا میتوان از همین تکنیک برای ترمیم نورونهای آسیبدیده پس از آسیب نخاع استفاده کرد. پترووا میگوید: «روشهای درمانی مبتنی بر این رویه، اغلب در زمینه درمان آسیبدیدگی نخاع نیز نتایج امیدوارکنندهای نشان میدهند. این امکان وجود دارد که افزایش تولید یا فعالیت پروترودین بتواند برای تقویت بازسازی در نخاع آسیبدیده استفاده شود.»
این پژوهش در مجلهی Nature Communications منتشر شده است.

اگر ترجیح میدهید برای بازی روی کامپیوتر، بهجای ماوس و کیبورد از کنترلر استفاده کنید، راهنمای خرید پیش رو برای شما است.

ارسال پیامهای دارای اسپویلر تلگرام بهخصوص در کانالهای عمومی برای مخفیکردن بخشی از متن یا حتی تصاویر، کاربرد دارد.

طبق مصوبهی ۳۰ دی ماه، هیئت دولت همه گوشیهای آیفون ۱۴ و ۱۵ و ۱۶ امکان رجیستر شدن دارند.

بانک مرکزی در نامهای کارگزاریهای رمزارزی را موظف کرد که ۱۰ ردیف اطلاعات خاص را در اختیار شاپرک قرار دهند تا درگاههای پرداختشان باز شود.

الگوریتم اینستاگرام در سال ۲۰۲۵ چطور کار میکند؟ اگر میخواهید بیشتر دیده شوید، زمانش رسیده است که رازهای الگوريتم جديد اينستاگرام را یاد بگیرید.

با بهترین برنامه پی دی اف ساز برای ایفون، اسناد کاغذی را در چند ثانیه دیجیتالی کنید. تجربهای حرفهای و سریع در انتظار شماست.

تیکتاک متعلق به شرکت چینی بایتدنس، از ۳۰ دی در ایالات متحده مسدود شد؛ پشت پردهی ماجرای ممنوعیت تیکتاک چیست و به کجا ختم میشود؟









































































