آیا mRNA علاوهبر واکسن، در درمان بیماریها نیز کاربرد دارد؟
موفقیت چشمگیر دو واکسن کووید ۱۹ در کارآزماییهای بالینی پیروزی بزرگی برای فناوری پزشکی است که قبلا اثبات نشده بود. هفتهی گذشته، یکی از این واکسنها مجوز استفادهی اضطراری را از سازمان غذا و داروی آمریکا دریافت کرد. واکسنهای مذکور متکیبر دستورالعملهای ژنتیکی هستند که با عنوان RNA پیامرسان (mRNA) شناخته میشود. این دستورالعملها سلولها را به ساخت یکی از پروتئینهای SARS-CoV-2 وادار میکند که سیستم ایمنی را برای شناسایی ویروس آموزش میدهد.
مدتها پیش از دنیاگیری کووید ۱۹، mRNA بهعنوان راهی ساده و انعطافپذیر برای تحویل واکسن و دارو در نظر گرفته میشد. توالی خاصی از mRNA ممکن است با تولید پروتئین تحریککنندهی رشد عروق خونی، قلب آسیبدیده را ترمیم کند. همچنین، توالی دیگر ممکن است آنزیمی را رمزگذاری کند که بتواند بیماری ژنتیکی نادری را معکوس کند.
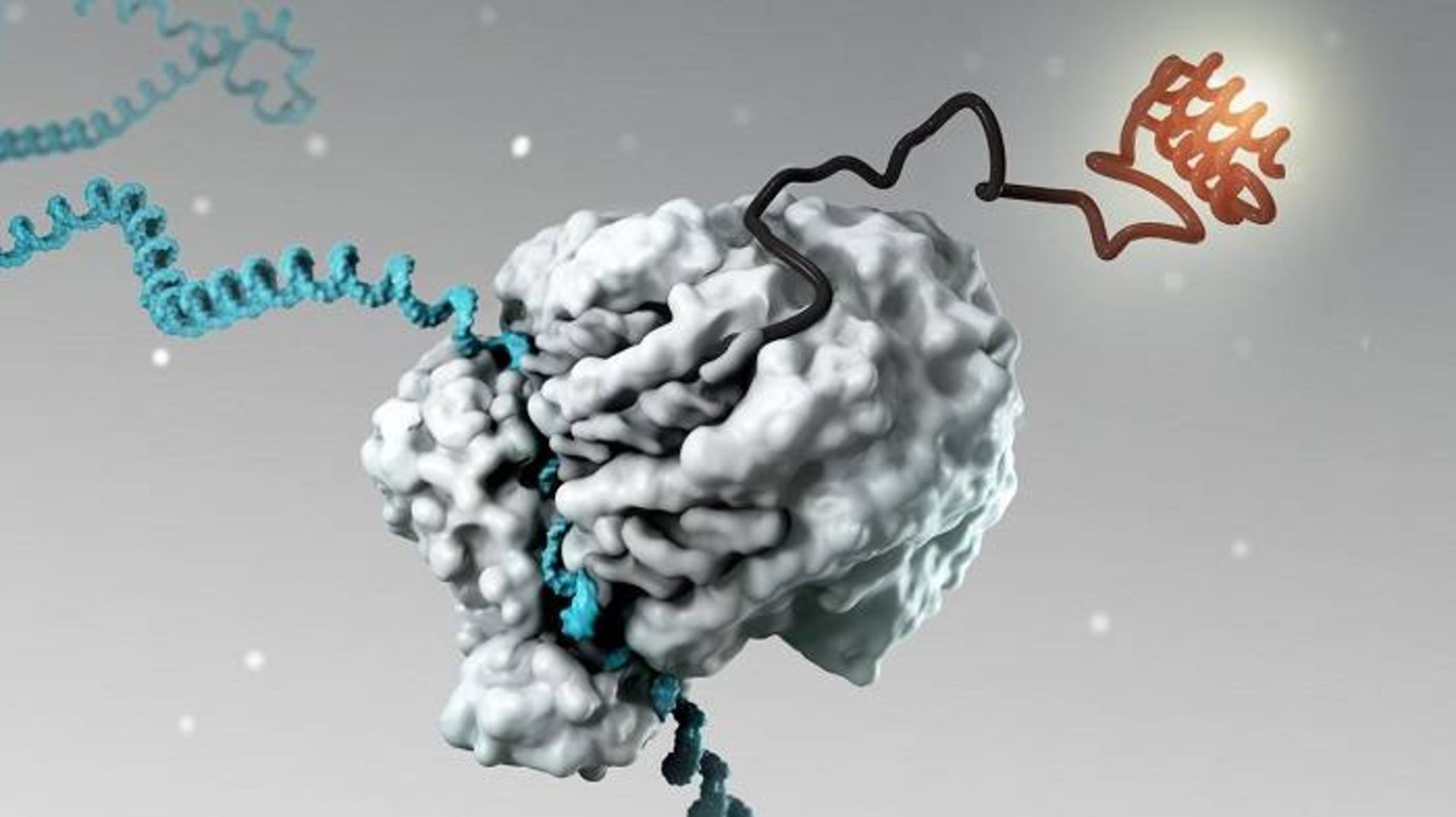
RNA پیامرسان (آبی) ریبوزومهای سلول را برای ساخت پروتئینهای جدید (قرمز) هدایت میکند
گوراو ساهای، دانشمند داروساز دانشگاه ایالتی اورگن، میگوید موفقیت واکسنهای کووید طوفانی از اشتیاق را درزمینهی این مفهوم ایجاد کرده است. بااینحال، داروهای mRNA بهویژه داروهایی که پروتئینهای مفید را برای بیماریهای مزمن جایگزین پروتئینهای معیوب میکنند، درمقایسهبا واکسنها مسیر سختتری برای رسیدن به کلینیکها پیش رو دارند. این داروها با چالش هدفگذاری mRNA برای بافتهای خاص و دادن مزایای قوی و پایدار بدون عوارض جانبی بیشازحد مواجه هستند.
موارد معدودی از درمانهای مذکور وارد کارآزماییهای بالینی شدهاند. هلین دویته، دانشمند داروساز دانشگاه گنت بلژیک میگوید: «اینطور نیست که توالی دیگری را وارد بدن کنید و هر چیزی درمان شود.» تطبیق داروی mRNA برای هر بیماری اغلب بهمعنای دستکاری ساختارهای خود mRNA و حباب محافظی است که برای انتقال آن به بدن استفاده میشود و نانوذرهی لیپیدی نام دارد.
برای واکسنها و برخی از داروهای mRNA استعمال نسبتا ساده است: پس از تزریق در بازو، سلولهای عضله mRNA را میگیرند و پروتئین ویروسی را تولید میکنند و درادامه، سیستم ایمنی پروتئین حاصل را بهعنوان عامل خارجی میبیند و آنتیبادیها و سلولهای T تولید میکند که بدن را برای دفاع دربرابر حملهی آینده آماده میکند. علاوهبر SARS-CoV-2، واکسنهای mRNA علیه هاری، زیکا، سیتومگالوویروس، آنفلوانزا و ویروسهای دیگر در کارآزماییهای بالینی در حال پیشرفت هستند.
همچنین، تزریق موضعی به عضله یا زیر پوست یا داخل تومور میتواند درمانهای مبتنیبر mRNA را به بدن تحویل دهد که سیستم ایمنی را برای مبارزه با سرطان بهکار میگیرد. چندین کارآزمایی بالینی برای چنین درمانهایی در حال انجام است که پروتئینهای تومور یا مولکولهای پیامرسان ایمنی را رمزگذاری میکنند تا به تشدید حمله بدن به سلولهای سرطانی کمک کند.
اگرچه کارآزماییهای متعددی در حال آزمایش RNA پیامرسان برای مسلحکردن سیستم ایمنی دربرابر ویروسها یا سرطان هستند، فقط چند شرکت کارآزماییهای بالینی کوچکی برای درمانهای دیگر (مانند استفاده از mRNA برای جایگزینکردن پروتئینهای ازدسترفته یا معیوب) آغاز کردهاند. در جدول زیر، به برخی از این شرکتها اشاره شده است.
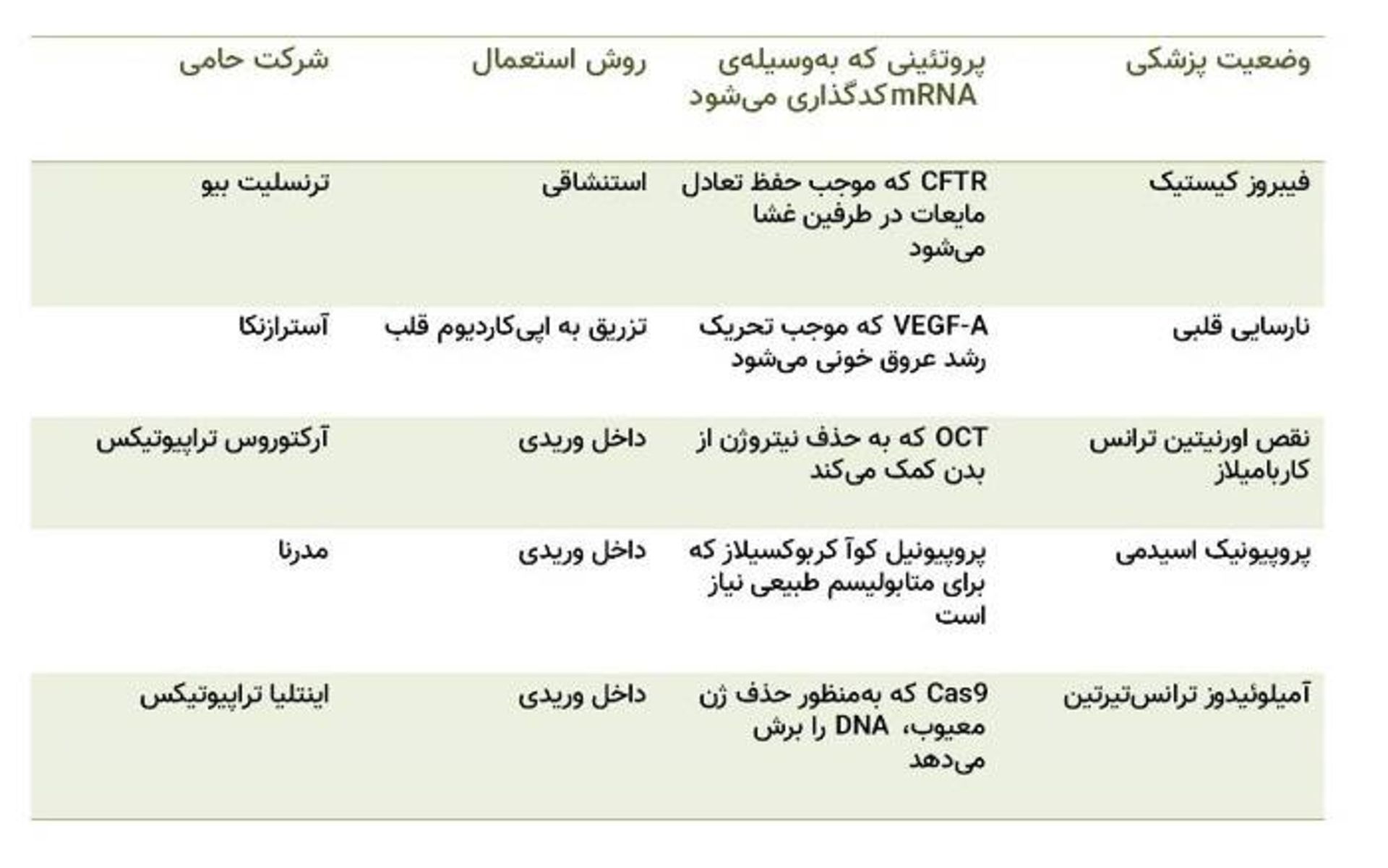
بسیاری دیگر از داروهای mRNA باید ازطریق جریان خون به مکان خاصی از بدن برسند. یک مورد نقص اورنیتین ترانس کاربامیلاز (OTC) است که فقدان آنزیمی موجب تجمع آمونیاک در خون میشود و به تشنج و کما و مرگ میتواند منجر شود. برای پیشگیری از تجمع آمونیاک، داروی mRNA باید به سلولهای کبد برسد.
شرکت آرکتوروس درزمینهی داروهای mRNA فعالیت میکند و یکی از اهدافش درمان OTC است. بهگفتهی جوزف پین، رئیس شرکت یادشده، این شرکت قصد دارد با تنظیم اندازه و بار الکتریکی نانوذرات لیپیدی مقدار دارویی را به حداکثر برساند که به کبد میرسد. شرکت آرکتوروس مطالعهی ایمنی اولیه را درحدود سی داوطلب سالم بهاتمام رسانده است و این ماه، دوازده فرد مبتلا به نقص مذکور داروی شرکت را دریافت کردند. از علل تمرکز آرکتوروس روی نقص OTC این بود که کبد معمولا ذرات را از جریان خون بهدام میاندازد و آنها را جمع میکند که نانوذرات درمانی را نیز شامل میشود.
جیمز دهلمن، متخصص مهندسی زیستپزشکی در مؤسسهی فناوری جورجیا، میگوید رساندن mRNA به بافتهای دیگر سختتر است. گروههای پژوهشی مختلفی مشغول دستکاری ساختار نانوذرات لیپیدی یا مزینکردن آنها با مولکولهایی هستند که آنها را بهسوی ارگان یا سلولهای خاصی هدایت میکند. آزمایشگاه دهلمن و شرکت گاید تراپیوتیکس (Guide Therapeutics) که او از بنیانگذارانش است، تکنیکی برای ردیابی مسیر هزاران نانوذرهی منحصربهفرد ازنظر شیمیایی با برچسبگذاری آنها با بارکدهای DNA ایجاد کرده است. بااینحال، او میگوید کشف ارتباط میان ساختار نانوذرهی لیپیدی و مقصدش یک دهه طول خواهد کشید.
دومین تفاوت بزرگ میان واکسنها و درمانهای مبتنیبر mRNA آن است که واکسنها فقط به یک یا چند دُز نیاز دارند. وقتی سیستم ایمنی برای حمله به تهدید مدنظر آموزش دید، پروتئین تولیدشده از mRNA تخریب میشود و به جایگزینی مجدد نیاز ندارد.
بهگفتهی دهلمن، داروهای mRNA که تاکنون به کارآزماییهای بالینی رسیدهاند، در بیشتر مواقع داروهایی هستند که اثر دارو بیش از طول عمر دارو است. این وضعیت برای روشهایی درمانی نیز وجود دارد که از mRNA برای رمزگذاری پروتئینهایی مانند آنزیم Cas9 استفاده میکند. آنزیم Cas9 ژنوم برای ایجاد ویرایشهای دائمی برش میدهد.
اینتلیا تراپیوتیکس (Intellia Therapeutics)، شرکت فعال درزمینهی ویرایش ژنوم به روش کریسپر، روی درمان مبتنیبر mRNA برای بیماری ارثی آمیلوئیدوز ترانستیرتین کار میکند. این شرکت داروی خود را ماه گذشته به اولین شرکتکننده کارآزمایی بالینی داد.
وقتی برای تأمین مجدد پروتئین در طول زندگی به تکرار دُزهای mRNA نیاز باشد، عوارض جانبی (احتمالا ناشی از تجمع نانوذرات لیپیدی در بدن یا پاسخ التهابی به RNA خارجی) بزرگتر میشود. آن باربیر، از شرکت ترنسلیت بیو (Translate Bio)، شرکت فعال درزمینهی درمانهای mRNA میگوید: «مردم ممکن است یکیدو روز ناراحتی و تب را پس از دریافت واکسن کووید ۱۹ را بپذیرند؛ اما اینکه این وضعیت را در تمام طول عمرتان هر سه هفته یک بار یا بیشتر تحمل کنید، پیشنهاد متفاوتی است.»
شرکت ترنسلیت بیو و شرکتهای دیگر برای اینکه دُزهای مکرر دارو قابلتحملتر باشد، مشغول طراحی mRNA هستند که تاحدممکن برای بدن طبیعی بهنظر برسد و آن را ازطریق نانوذرات زیستتخریبپذیر تحویل میدهند. درمان mRNA شرکت ترنسلیت بیو برای فیبروز کیستیک اکنون در مرحلهی آزمایشهای بالینی است. بهگزارش این شرکت، یک دُز واحد از این درمان عارضهی جانبی جدی بههمراه نداشت؛ ولی برخی بیماران دچار تب و درد عضلانی یا سردرد شدند که کوتاهمدت و مهارشدنی بود. گفتنی است کارآزمایی دیگری نیز در حال آزمایش دُزهای متعدد است.
افزایش مقدار پروتئینی که بدن از یک دُز mRNA میسازد، موجب کاهش فراوانی و اندازهی دُزهای موردنیاز میشود. ساهای میگوید یکی از روشها آن است که توانایی نانوذرات لیپیدی را در فرار از آن دسته از کیسههای غشایی افزایش دهیم که سلول برای گیرانداختن آنها استفاده میکند. بدینترتیب، مقدار بیشتری از محمولهی mRNA نانوذرات فرصتی برای تعامل با ماشینآلات سلولی برای ساخت پروتئین پیدا میکند. تیم وی ماه فوریه گزارش کرد که در آزمایشهای انجامشده روی سلولها، گنجاندن انواع طبیعی کلسترول در نانوذرات لیپیدی موجب شد آنها بتوانند بهتر فرار کنند.
رقابت برای ساخت واکسن mRNA علیه کووید ۱۹ مشکلات تحویل و استعمال مکرر درمانهای mRNA را برطرف نکرده است؛ اما شاید مسیر آنها را ازطریق دیگری هموار کرده باشد. موضوعی که تولیدکنندگان واکسن نشان دادهاند، این است که تولید میلیاردها نانوذره و رشتهی mRNA در زمان کوتاهی امکانپذیر است. تیم ساهای هنوز در حال کشف بهترین نانوذرات لیپیدی برای همراهی و رساندن mRNA به بخشهای دورازدسترس بدن است. او رسیدن به چنین کشفی را تحولآفرین میخواند؛ چراکه اکنون مراحل رسیدن این درمانها به کلینیک هموار شده است.