آیا نوعی پروتئین جادویی میتواند روند پیری را آهسته کند؟

چندین سال پیش، دانشمندانی که در مؤسسه سلولهای بنیادی هاروارد روی پیری مطالعه میکردند، از تکنیکی به نام پارابیوز (متصلکردن موش جوان به موش پیر بهکمک جراحی با هدف داشتن خون مشترک) بهمنظور بررسی این مسئله استفاده کردند که برای بافت عضله اسکلتی و قلب چه اتفاقی میافتد. آنان از پژوهشهای گذشته میدانستند که قراردادن خون جوان در موشهای پیر موجب میشود که موشهای پیر ازنظر زیستی جوانتر شوند و موشهای جوانی که درمعرض خون پیر قرار میگیرند، سریعتر پیر میشوند.
ایمی ویجرز و ریچارد لی، پژوهشگران دانشگاه هاروارد، دریافتند که بافت قلب موش پیر ترمیم و جوان شده بود. درواقع، اندازه قلب موش پیر کاهش پیدا کرده بود و بهاندازه قلب موش جوان رسیده بود. لی رابین، استاد پزشکی ترمیمی و سلولهای بنیادی در هاروارد و یکی از مدیران برنامه علوم اعصاب مؤسسه سلولهای بنیادی گفت: «همه ما تعجب کردیم. ماده جادویی موجود در خون چه بود؟»
ماده جادویی که آنها شناسایی کردند، پروتئینی به نام GDF11 بود که یکی از دههاهزار پروتئینی است که در بدن انسان تولید میشود. همچنین، آزمایشگاه دکتر رابین دریافت که GDF11 در موشها باعث تحریک رشد عروق خونی جدید در مغز و تولید سلولهای عصبی جدید در هیپوکامپ میشود. هیپوکامپ بخشی از مغز است که با یادگیری و حافظه ارتباط دارد. آزمایشگاه دکتر ویجرز دریافت که GDF11 بافت عضلات اسکلتی را نیز جوان کرده بود. یافتههای دانشمندان در سالهای ۲۰۱۳ و ۲۰۱۴ در مجله Science منتشر شد.
سؤال واضح بعدی این بود که آیا میتوان از GDF11 بهمنظور تحریک بازسازی و ترمیم در انسان استفاده کرد؟ در سال ۲۰۱۷، دکتر رابین و دکتر ویجرز و دکتر لی بههمراه پنج فرد دیگر استارتاپ الیوین (Elevian) را با هدف تجاریسازی درمانهای مبتنیبر GDF11 بهمنظور متوقف و کُند یا معکوس کردن بیماریهای مرتبط با پیری تأسیس کردند. دکتر مارک آلن، مدیر اجرایی الیوین گفت:
ما به پروتئینهایی مانند GDF11 علاقهمند هستیم که وارد جریان خون میشوند؛ زیرا آنها میتوانند تغییراتی در کل بدن ایجاد کنند و این نوع تغییراتی است که ما میخواهیم.
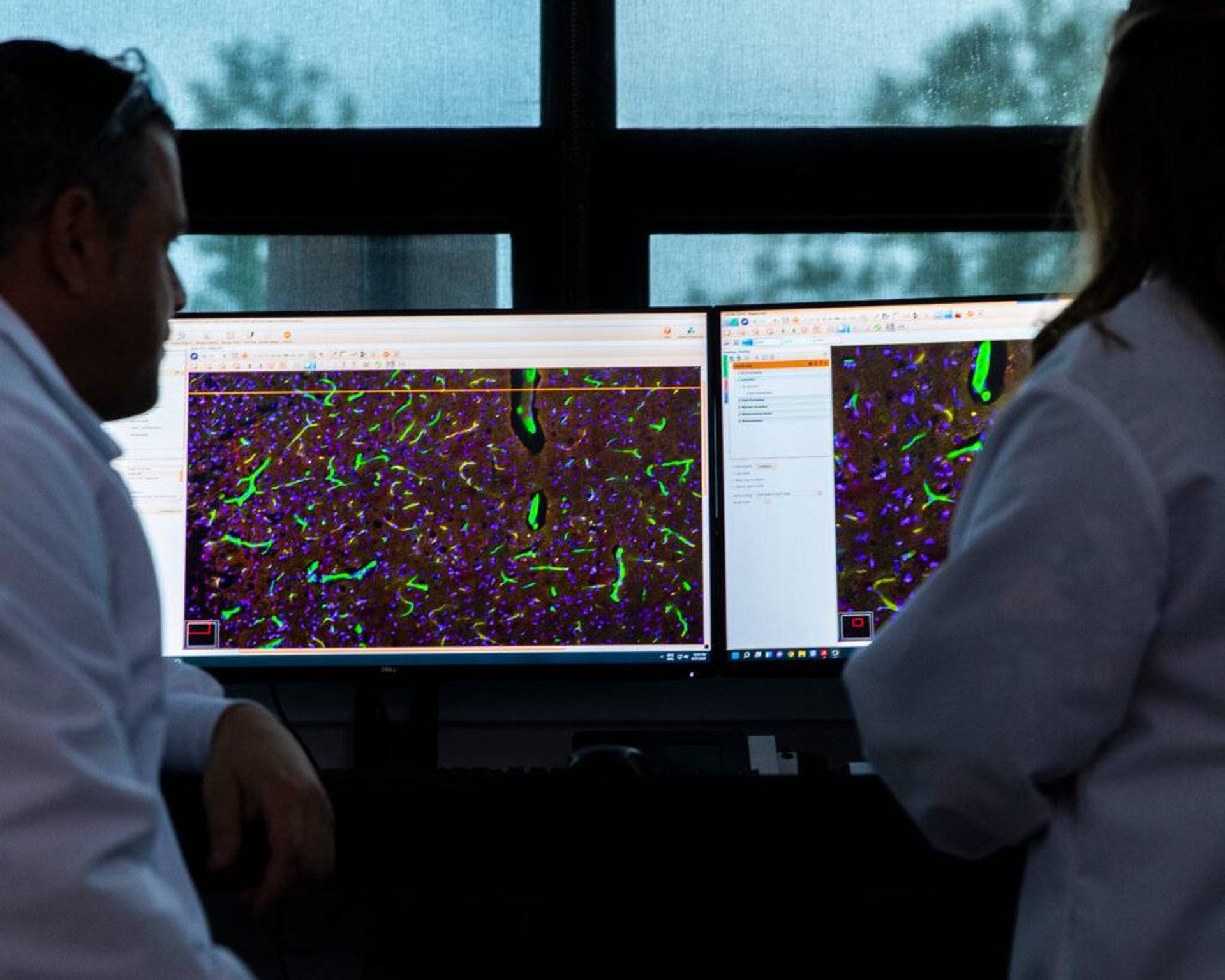
دانشمندان در دفتر مرکزی الیوین به نشانگرهای تشکیل نورونهای جدید در موشهای درمانشده با GDF11 نگاه میکنند.
دکتر آلن اولین شرکت مراقبتهای بهداشتی خود را زمانی راهاندازی کرد که در دانشکده پزشکی دانشگاه کالیفرنیا در لسآنجلس مشغول به کار بود. او در سال ۲۰۰۰ موقعیت شغلی خود را ترک کرد تا شرکت دوم را راهاندازی کند. در اوایل سال ۲۰۱۷، دکتر آلن و شریکش، سباستین گیوا، بهدنبال راهاندازی شرکت جدیدی بودند تا درمانهایی را توسعه دهد که فرایندهای تخریبکننده مرتبط با پیری را هدف قرار دهد. آنان پیش از اینکه تصمیم بگیرند روی GDF11 کار کنند، چندین پروژه پژوهشی بالقوه را بررسی کردند. دکتر آلن گفت:
این ایده را داشتم که خود پیری میتواند هدفی برای مداخله درمانی باشد؛ زیرا اگر یکی از جنبههای پیری را هدف قرار دهیم، قابلیت درمان بیماریهای مختلفی را خواهیم داشت.

لی رابین، استاد سلولهای بنیادی و پزشکی ترمیمی در هاروارد و یکی از مدیران برنامه علوم اعصاب مؤسسه سلولهای بنیادی دانشگاه هاروارد. آزمایشگاه دکتر رابین دریافت که GDF11 در موشها موجب تحریک رشد عروق خونی جدید در مغز میشود.
پژوهشهای اولیه درباره خواص جوانسازی GDF11 با واکنشهای منفی جامعه علمی مواجه شد. در سال ۲۰۱۵، پس از اینکه دکتر ویجرز و دکتر لی نتایج خود را منتشر کردند، گروهی از پژوهشگران به رهبری دیوید گلس که در آن زمان مدیر اجرایی مؤسسه تحقیقات زیستپزشکی نوارتیس در کمبریج ماساچوست بود، صحت یافتههای آنها را در مقالهای در مجله Cell Metabolism رد کردند. در پی آن، پژوهشگران هاروارد در مقاله دیگری که اواخر همان سال در مجله Circulation Research منتشر شد، یافتههای تیم نوارتیس را نقد و به مشکلی در یافتههای تیم نوارتیس اشاره کردند.
دکتر گلس که اکنون در شرکت بیوتکنولوژی ریجنران مشغول به کار است، اخیراً در ایمیلی گفته است از پژوهش اولیه خود حمایت میکند که نشان داد GDF11 بهجای کمک به بازسازی عضلات بازسازی را مهار میکند. بااینحال، او افزود: «پژوهش ما همچنان این احتمال را باقی میگذارد که در برخی شرایط، GDF11 ممکن است اثرهای مثبتی داشته باشد.»
دکتر آلن گفت از زمان اختلافنظر اولیه، تیم پژوهشی الیوین یافتههای اولیهاش را در چند مطالعه تکرار کرده است؛ اما هیچیک هنوز در مجلهای معتبر منتشر نشده است. این در حالی است که مؤسسههای غیرمرتبط با الیوین مطالعات پیشبالینی زیادی انجام داده و منتشر کردهاند که اثربخشی درمانی rGDF11 (فرمی از GDF11 که در آزمایشگاه تولید شده است) را در درمان بیماریهای وابستهبه سن نشان دادهاند.
الیوین در مسیر آغاز کارآزماییهای بالینی انسانی در سهماهه نخست سال ۲۰۲۳ قرار دارد و ۵۸ میلیون دلار سرمایه جمعآوری کرده است. شرکت الیوین یکی از شرکتهای متعددی است که تلاش میکنند راههایی برای افزایش طول عمر سالم انسان پیدا کنند؛ یعنی دورهای از زندگی که فرد بهطورکلی در وضعیت سلامتی خوبی قرار دارد.
این بخش نوظهور از صنعت داروسازی اغلب «درمانهای طول عمر» نامیده میشود و شامل شرکتهایی مانند Altos Labs ،Calico Life Sciences ،Unity Biotechnology ،Alkahest و Juvenescence میشود. بهگزارش شرکت تحقیقاتی Longevity Technology، در سال ۲۰۲۱، حدود ۲ میلیارد دلار در شرکتهای داروسازی مختلف روی رویکردهای ضدپیری سرمایهگذاری شد.

از سمت چپ: اسکن سلولهای مغز موش که با GDF11 درمان شده است؛ ابزارهای خالصسازی استفادهشده برای استخراج پروتئین GDF11 و دانشمندی که در آزمایشگاه دکتر رابین کار میکند.
پژوهشگران سالها بهدنبال داروهایی بودهاند که بتواند طول عمر را افزایش دهند. ۱۷ سال پیش، برنامه Interventions Testing Program در مؤسسه ملی سلامت آزمایش داروهای مختلفی را در موشها آغاز کرد تا ببیند که آیا این مداخلات طول عمر آنها را افزایش میدهد. دکتر ریچارد میلر، استاد آسیبشناسی دانشگاه میشیگان و مدیر مرکز تحقیقات زیستشناسی پیری پل اف گلن، گفت درمانهای ضدپیری اغلب روی موشها آزمایش میشود؛ زیرا پیری در موشها بسیار شبیه پیری در انسان است. او گفت:
موشها و انسانها ازنظر اعضا و زیستشناسی سلولی و بیشتر انواع نورونها و انتقالدهندههای عصبی باهم شباهت دارند و اغلب به روشهای مشابهی به داروها واکنش نشان میدهند.
مسئلهی مهمی که پیش روی همه این شرکتها قرار دارد، این است که تجاریسازی داروهای ضدپیری تقریباً غیرممکن است؛ زیرا سازمان غذا و دارو پیری را بهعنوان بیماری درمانپذیر بهرسمیت نمیشناسد. علاوهبراین، حتی اگر سازمان مذکور پیری را بهعنوان بیماری در نظر بگیرد، مطالعات بالینی موردنیاز برای تأیید موثربودن درمان سالها طول میکشد. دکتر میلر گفت:
احتمالاً مطالعات بالینی برای بررسی اینکه آیا داروی خاصی پیری را کُند میکند و از این طریق بسیاری از پیامدهای پیری را بهتأخیر میاندازد، زمان بسیار زیادی طول خواهد کشید.
بنابراین، بنیانگذاران الیوین به این نتیجه رسیدند که سریعترین راه برای بازاریابی GDF11 هدف قراردادن نوعی بیماری خاص است. دکتر آلن گفت:
فکر کردیم بدترین بیماری که درمان مناسبی ندارد و میتوانیم آن را در کوتاهترین زمان ممکن درمان کنیم و اثرهای بالینی را نشان دهیم، چیست؟ ما به این نتیجه رسیدیم که سکته مغزی هدف مناسبی است؛ زیرا علت اصلی ناتوانی طولانیمدت است و گزینههای درمانی بسیار محدودی دارد.
دکتر الیزابت بریس مارش، مدیر پزشکی برنامه جامع سکته مغزی در مرکز پزشکی بیویو دانشگاه جانز هاپکینز، گفت بهترین درمان برای سکته ناشی از لخته خون (حدود ۸۷ درصد از موارد سکته) نوعی دارو است که فعالکننده بافتی پلاسمینوژن یا tPA نامیده میشود. این دارو باید ۴/۵ ساعت بعد از زمان سکته تجویز شود و لختههای بزرگ نیز باید بهکمک جراحی برداشته شوند.
بااینحال بهگفته کارشناسان، فقط حدود ۲۰ درصد از قربانیان سکته مغزی tPA را دریافت میکنند. دلیل این امر آن است که یا سکته آنان بهسرعت تشخیص داده نمیشود یا بیمار بهعلت مشکلات قبلی واجدشرایط دریافت دارو نیست. پژوهشگران الیوین گفتند مطالعات پیشبالینی آنان که هنوز منتشر نشده، نشان داده است که فقط چند روز درمان با GDF11 میتواند به بهبودی پس از سکته کمک کند. آنان دریافتند که GDF11 التهاب را کاهش میدهد و متابولیسم را بهبود میبخشد و مغز را برای بازتولید عروق خونی و نورونها تحریک میکند.

دکتر مارک آلن، مدیر اجرایی شرکت الیوین
مانع بزرگی بعدی الیوین افزایش مقیاس تولید است که به تجهیزات و شرایط ویژهای نیاز دارد. پژوهشهای بسیار زیادی در این شرکت در حال انجام است که ظرفیت تولید شرکت را اشغال کردهاند. دکتر آلن گفت:
آنان مشغول پژوهشهای مرتبط با کووید هستند و بهطورکلی، بودجه زیادی در بخش بیوتکنولوژی تأمین شده است بنابراین، یافتن فضایی که با شرایط موردنیاز ما مطابقت داشته باشد، دشوار است.
افزونبراین همچون بخشهای دیگر اقتصاد، پژوهشهای تکنولوژی با مشکلات زنجیره تأمین مواجه است و این امر دستیابی الیوین به مواداولیه موردنیاز برای انجام پژوهشها را دشوارتر میکند. بااینهمه، این شرکت با حداکثر سرعت ممکن حرکت میکند و دکتر آلن معتقد است که نتایج پژوهش آنها تأثیر عمیقی بر نحوه پیری ما و طول عمر خواهد گذاشت. او درپایان گفت:
با هدف قراردادن مکانیسمهای اساسی پیری، این فرصت را داریم که چندین بیماری مرتبط با پیری را درمان یا از آنها پیشگیری کنیم. ما میخواهیم عدد ۱۰۰ (سال) جایگزین ۵۰ شود.